细胞铺板与细胞计数标准化操作指南:实验流程、关键细节与误差控制技巧
发布时间:2026-04-10 浏览次数:57
细胞铺板与细胞计数是细胞生物学实验中最基础且关键的操作,其准确性直接决定后续实验结果的可靠性与可重复性,广泛应用于细胞培养、药物筛选、增殖检测等各类实验场景。本文将从核心原理、实验准备、实验步骤、数据分析处理四个维度,详细拆解标准化操作流程,助力科研人员规范实验操作、减少误差。

一、核心原理
1、细胞铺板:基于细胞粘附特性,将分散均匀的单细胞悬液接种至无菌培养容器,在新鲜培养基、血清等营养环境中实现贴壁生长,核心为控制适配培养容器的细胞密度,避免接触抑制或生长不足。
2、细胞计数:依托细胞计数板四大计数方格规格,将稀释后细胞悬液滴入计数区,通过显微镜计数结合稀释倍数,推算原细胞悬液密度;台盼蓝可区分死活细胞,提升计数准确性,无条件可省略。
二、实验准备
1、材料准备:核心材料包括显微镜、75% 酒精棉球、移液枪及枪头、PBS 液、血清、新鲜培养基、10mL 离心管、细胞培养皿、离心机、盖玻片、细胞计数板,需提前确认材料无菌、试剂有效;明确不同培养容器对应细胞量(如 6 孔板 10^6 个 /mL、96 孔板 10^4 个 /mL)。
2、环境准备:材料放入超净台后,提前 30 分钟开紫外灯灭菌,37℃预热培养基、PBS;紫外灭菌后,用 75% 酒精棉球全面擦拭超净台。
3、细胞准备:显微镜观察细胞,确认状态良好、处于生长对数期;通过文献、预实验等确定目标培养容器的铺板细胞密度与载体参数。

三、实验步骤
1、细胞收集与悬液制备:转移细胞悬液至标记 5mL 离心管,1000rpm 离心 3-5 分钟弃上清;加 1mL PBS 清洗后再次离心弃上清;加 1mL 培养基充分吹打,制备原细胞悬液。
2、细胞稀释与计数:吸 20μL 原细胞悬液 + 180μL 培养基,稀释 10 倍得稀释悬液;取 10μL 稀释悬液 + 10μL 台盼蓝混匀,用 10μl 枪头倾斜滴加至盖好盖玻片的计数板,确保计数区无气泡;低倍镜找计数视野,高倍镜按 “计上不计下、计左不计右” 计数四大方格细胞;重复计数 2 次取平均值。
3、细胞铺板:按 C1V1=C2V2 公式计算原细胞悬液需加体积;先加计算量的原悬液,补培养基至目标体积(如 6 孔板每孔 2mL);以 “十字” 形摇匀,镜下确认细胞均匀无气泡后,放入培养箱。

四、数据分析处理
1、细胞密度计算:稀释悬液密度 =(四大方格细胞总数 ÷4)×10^4 个 /mL;原悬液密度 = 稀释悬液密度 × 稀释倍数(如 10 倍则 ×10)。
2、铺板体积计算:以目标密度、每孔终体积为基础,计算原悬液体积,确保每孔终细胞数达标(如 6 孔板目标 1×10^6 个 /mL、终体积 2mL,需原悬液 1mL)。
3、异常处理:少量成团细胞按 1 个处理;成团过多需重新制备单细胞悬液;铺板后细胞结团,调整密度或改用 “8” 字摇匀法。
五、注意事项与常见问题
1、计数时,细胞混悬液加入计数板需缓慢,避免产生气泡;铺板摇匀时动作轻柔,防止细胞损伤和气泡产生。
2、若出现细胞结团,多为铺板密度过高或摇匀方法不当导致,可调整细胞密度,采用“十字”形或“8”字形摇匀。
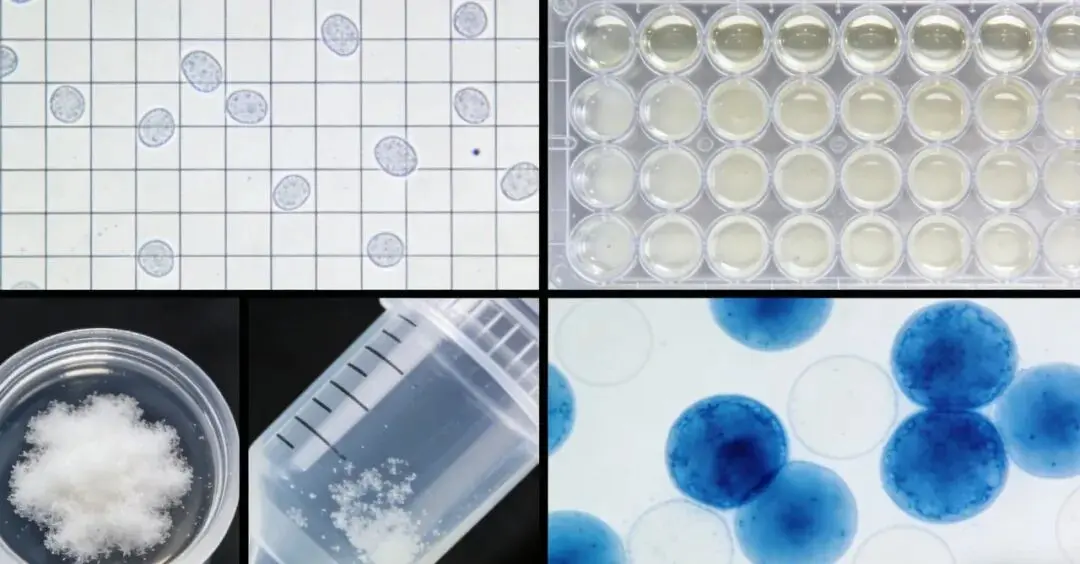
总结:细胞铺板与细胞计数的关键的是严格遵循无菌操作、把控细胞状态、规范计数流程和保证数据精准,守住这些核心细节,才能有效提升实验的可重复性,为后续实验奠定可靠基础。
本文由环凯转载自“医研学者”公众号,版权归原作者所有,仅供学习参考,如有侵权请联系删除!









