细胞冻存与复苏全攻略:慢冻快融原理、DMSO毒性及无血清冻存液对比
发布时间:2026-04-10 浏览次数:70
“细胞状态一直很好,冻了一批进液氮,三个月后复苏,全死了。” —— 这句话,几乎在每个细胞房都响起过。冻存与复苏看似简单,实则每一个细节都藏着“翻车点”:DMSO浓度、降温速度、复苏后要不要离心、何时换液……一个环节出错,数月的工作可能瞬间归零。今天,我们把细胞冻存复苏从头到尾掰开揉碎,讲透原理+配方对比+标准化操作,让你从此告别“玄学冻存”。
核心口诀:慢冻快融,细胞不哭;去毒离心,状态爆棚。
一、冻存的底层逻辑:为什么必须“慢冻快融”?
冻存的核心目标是:让细胞在超低温下暂停生命活动,同时保证复苏后还能活过来。最大的敌人——冰晶。当温度下降时,细胞内水分结冰,若降温过快,细胞内形成尖锐冰晶刺破细胞膜;降温过慢,细胞长时间暴露在高渗环境中因渗透压失衡死亡。“慢冻”让水分有足够时间渗出胞外,在胞外形成冰晶,保护胞内结构。而复苏时则相反:必须快速融化,避免重结晶造成二次损伤。经典法则:慢冻快融,细胞不哭。
二、DMSO深度解析:冻存液的核心与“双刃剑”
2.1 DMSO为什么不可或缺?
DMSO(二甲基亚砜)是目前最常用的渗透性冷冻保护剂,它能降低冰点、置换细胞内水分、稳定膜结构,没有DMSO绝大多数哺乳动物细胞无法成功冻存。
DMSO的“毒性”真相 —— 最新研究揭示(Cryobiology 2024):使用10% DMSO冻存人骨髓间充质干细胞,复苏后立即有10-15%细胞发生凋亡,培养48小时DNA损伤/修复信号是新鲜细胞的3.8倍,同时细胞内活性氧(ROS)水平显著升高,成脂/成骨分化能力及迁移能力均下降。DMSO处理本身就造成基因组损伤和功能削弱。
2.2 如何降低DMSO损伤?
- 复苏后尽快离心去除:解冻后立即用5倍体积培养基稀释并离心(90-110×g,5min)。
- 优化浓度:常规10%,敏感细胞可降至5-7.5%(配合其他保护剂如海藻糖)。
- 复苏后24小时内换液:清除残留DMSO,避免持续毒性。
三、传统冻存液 vs 无血清冻存液:选对配方,事半功倍
对比维度 | 传统冻存液(含血清) | 无血清冻存液 |
|---|---|---|
| 成分 | 90%完全培养基+10% DMSO(或70%基础+20%FBS+10%DMSO) | 化学成分明确:渗透性保护剂(DMSO)+非渗透性保护剂(海藻糖/蔗糖/PVP)+氨基酸/维生素,无动物源组分 |
| 冻存操作 | 必须程序降温(4℃→-20℃→-80℃→液氮或异丙醇冻存盒,约1℃/min) | 直接放入-80℃,无需程序降温,24h后转液氮即可 |
| 复苏存活率 | 一般,微量冻存时不稳定 | 高且稳定,尤其适合微量/珍贵细胞 |
| 批次差异 | 大(血清批次影响显著) | 极小,化学成分确定 |
| 安全性 | 存在支原体/病毒污染风险 | 无动物源污染风险 |
| 整板冻存 | 不可行 | 可行,均一性好 |
| 成本 | 极低 | 较高(传统配方的5-10倍) |
3.1 无血清冻存液:为什么能“直接扔-80℃”?
核心在于非渗透性保护剂(海藻糖、蔗糖、PVP等)在细胞外形成保护层,辅助细胞脱水,协同DMSO降低冰晶形成风险,即使降温速度不均匀也能存活。此外,市售优质无血清冻存液大多含抗氧化因子,可进一步减轻ROS损伤。适合无血清培养的细胞、原代细胞、干细胞以及追求高效率的实验室。
缺点提醒:①成本较高;②大多数产品仍含DMSO(5-10%),毒性问题依然存在;③极少数原代细胞可能不如定制配方理想;④-80℃长期保存(>1年)仍建议转液氮。
四、标准化冻存操作流程(慢冻版·通用黄金标准)
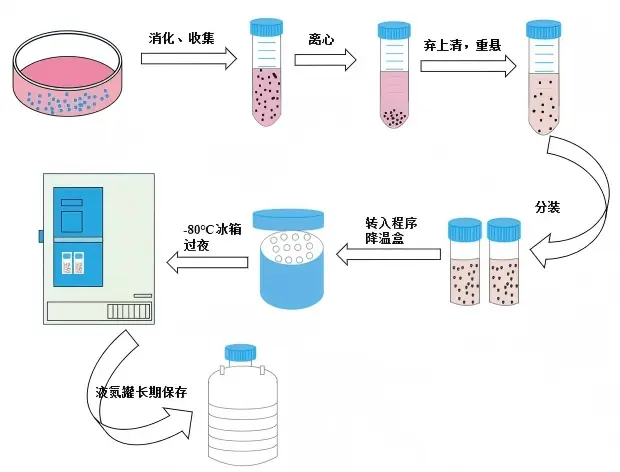
冻存前准备:
细胞状态:对数生长期,密度80-90%,活力>90%;冻存液提前预冷(传统配方需4℃预冷);胰酶、PBS、完全培养基37℃预热。
✅ Step 1 制备细胞悬液
吸弃旧培养基 → PBS洗2次 → 胰酶消化(镜下观察1-2min)→ 完全培养基终止 → 轻轻吹打 → 离心200-400×g,3-5min。
✅ Step 2 加入冻存液 & 分装
弃上清,加入适量冻存液重悬,调整密度至 1×10⁶ ~ 5×10⁶ cells/mL,分装至冻存管(1mL/管),标记细胞名称、代数、日期。
✅ Step 3 降温程序
传统冻存液:4℃ 10min → -20℃ 30min → -80℃ 过夜 → 次日转液氮。
无血清冻存液:直接放入-80℃冰箱,24h后转入液氮(可长期保存)。
提示:异丙醇冻存盒可替代程序降温仪,确保-80℃时约-1℃/min的降温速率。
五、复苏标准化操作:快速解冻 + 离心去毒
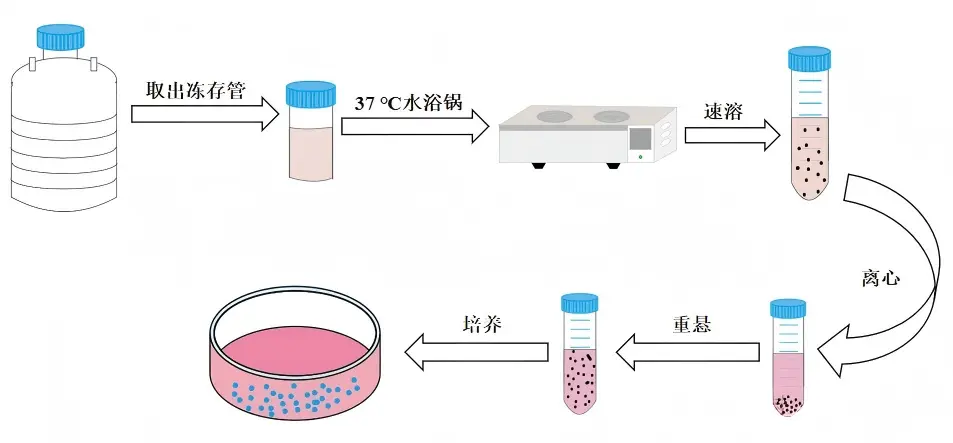
第1步:37℃水浴快速解冻(1-2分钟)
从液氮取出冻存管,立即放入37℃水浴,轻摇至仅剩小冰晶(切勿超过3min),75%酒精擦拭管壁后移入超净台。
第2步:离心法去除DMSO(推荐)
将细胞悬液移入离心管 → 缓慢加入5倍体积预热的完全培养基(沿管壁,避免渗透冲击)→ 轻轻混匀 → 离心 90-110×g,5min → 弃上清(含DMSO的死细胞混合物)。
第3步:重悬 & 接种
加入1-2mL预热完全培养基重悬 → 接种至培养皿/瓶 → 补足培养基 → 置于培养箱。
第4步:复苏后24小时必须换液
复苏后24h吸弃旧培养基(含残留DMSO及死细胞碎片)→ 更换新鲜完全培养基 → 继续培养。此步骤极大提升细胞活力与增殖率。
直接铺板法(不离心)可行吗? 仅当冻存液中DMSO浓度足够低,使最终培养基中DMSO<0.4%时可尝试,但敏感细胞(原代、干细胞)必须离心去除DMSO,否则贴壁及存活率显著下降。
六、常见问题与避坑指南(实战锦囊)
- 复苏后贴壁差怎么办?
提前用胶原/多聚赖氨酸包被培养皿;降低离心力至70-80×g;提高接种密度;添加10% FBS+生长因子;干细胞可加ROCK抑制剂(Y-27632)。
- -80℃能存多久?必须转液氮吗?
无血清冻存液:-80℃可保存至少1年;传统冻存液建议2周内转入液氮。长期保存必须液氮(-196℃),避免冰晶重排。
- 敏感细胞(NK、干细胞)如何优化?
降低DMSO至5-7.5%+海藻糖;使用程序降温仪;复苏时添加血清并采用梯度稀释离心法;使用低DMSO或无DMSO商品化冻存液(如含羟乙基淀粉等)。
- 冻存液可以反复冻融吗?
严禁反复冻融,应分装保存,传统冻存液现配现用,无血清冻存液2-8℃保存即可,不可反复回温。
七、一张表总结:根据场景选对冻存策略
应用场景 | 推荐方案 | 理由 |
|---|---|---|
常规细胞系,预算有限 | 传统冻存液 + 程序降温(异丙醇盒) | 成本极低,效果稳定 |
常规细胞系,追求便捷高效 | 无血清冻存液 | 直接-80℃,省时省力,存活率高 |
无血清培养细胞 | 无血清冻存液 | 避免血清干扰,无需驯化 |
原代细胞/干细胞/类器官 | 无血清冻存液 + 程序降温仪(或含ROCKi) | 最大限度保留分化潜能,低DMSO损伤 |
整板冻存/高通量筛选 | 无血清冻存液 | 均一性好,适合大规模冻存 |
临床级细胞治疗 | 低DMSO或无DMSO专用冻存液 | 避免输注不良反应,符合GMP规范 |
核心总结:深度理解冻存、复苏过程,每一步都有分子层面的依据。
✅ DMSO不可或缺但有毒,复苏后必须尽快离心去除;
✅ 无血清冻存液省去程序降温,化学定义明确,是现代化细胞培养的利器;
✅ “慢冻快融+24h换液”是永恒的黄金法则;
✅ 根据细胞类型和实验目的选择冻存体系,可最大限度降低细胞株丢失风险,让每一份冻存的细胞都成为可靠的“种子库”。
本文由环凯转载自“艾思力克”公众号,版权归原作者所有,仅供学习参考,如有侵权请联系删除!










