细胞共培养方法有哪些?4种主流 Co-culture 技术对比与选型指南
发布时间:2026-04-21 浏览次数:29
作为一名科研党,你是否曾苦恼于单细胞培养无法还原体内复杂的微环境?细胞共培养(Co-culture)技术正是打破这一局限的神兵利器。
今天,我们就来盘点目前市面上主流的四种细胞共培养方法,帮你快速锁定最适合你实验的那一款!
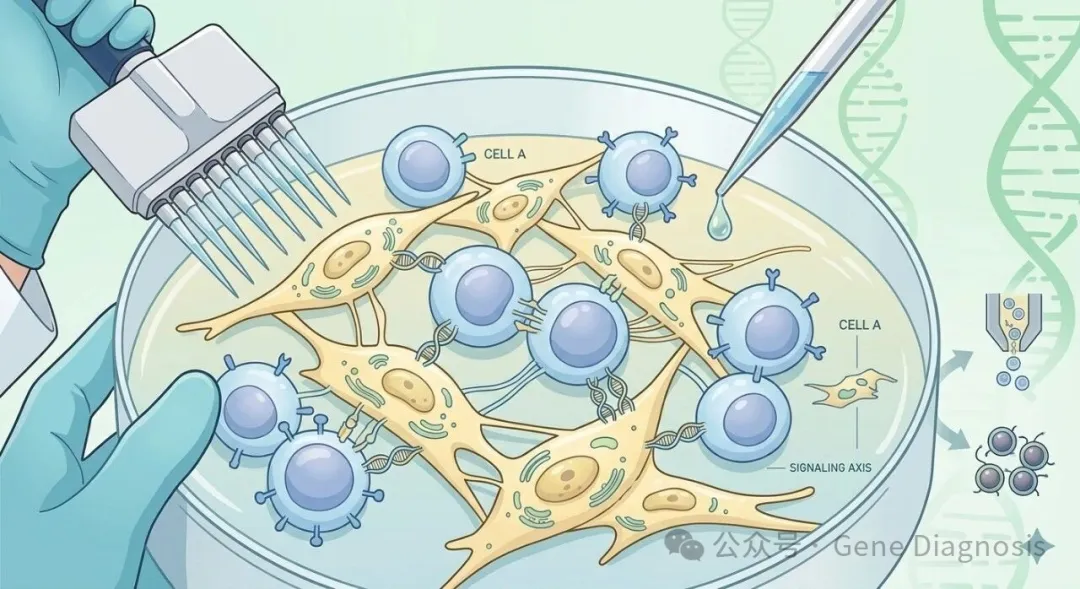
01、直接共培养 (Direct Co-culture)
原理: 将两种或多种细胞直接混合接种在同一个培养皿中,细胞之间可以发生物理接触。
优点: 最真实地模拟了细胞间的接触信号传导;操作极其简单,成本最低。
缺点: 两种细胞混在一起,后期很难通过简单的消化将它们完全分离(除非使用流式分选或磁珠分选)。
适用方向: 免疫细胞杀伤实验、细胞间物理接触通讯研究。
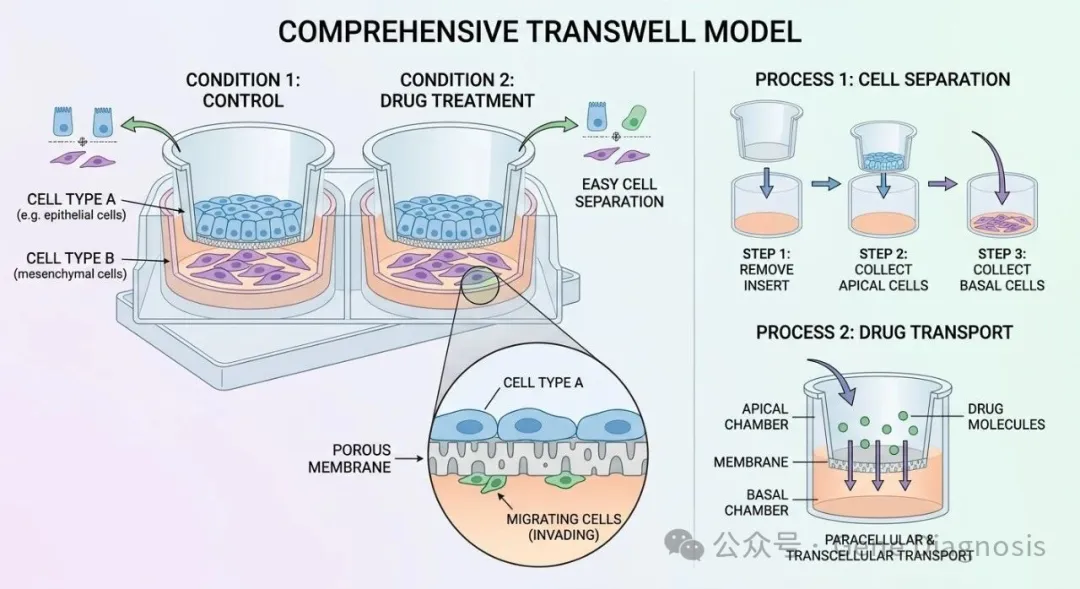
02、Transwell 间接共培养
原理: 利用带有多孔膜的嵌入式小室(Insert)。一种细胞种在小室上层,另一种种在孔板底部。
优点: 细胞互不接触,但代谢产物和分泌因子(如外泌体、细胞因子)可以自由穿过多孔膜。实验结束后,上、下层细胞可轻松分离进行后续检测。
缺点: 无法模拟细胞间的物理接触;分泌因子会被大量的培养基稀释。
适用方向: 细胞迁移/侵袭实验、旁分泌信号传导、药物转运研究。
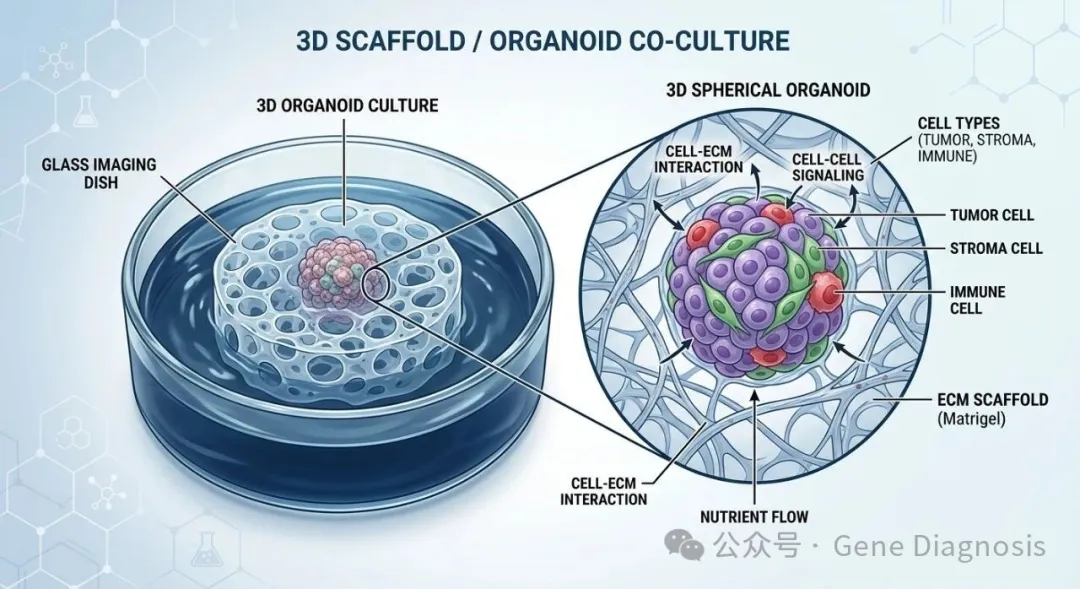
03、3D 支架/类器官共培养
原理: 将细胞包裹在水凝胶(如Matrigel)或生物支架中,模拟体内的三维空间结构。
优点: 极高地还原了体内组织形态和细胞外基质(ECM)环境,结果更具临床参考价值。
缺点: 技术门槛高,细胞回收困难,观察(显微成像)难度大,成本昂贵。
适用方向: 肿瘤微环境模拟、类器官构建、组织工程。
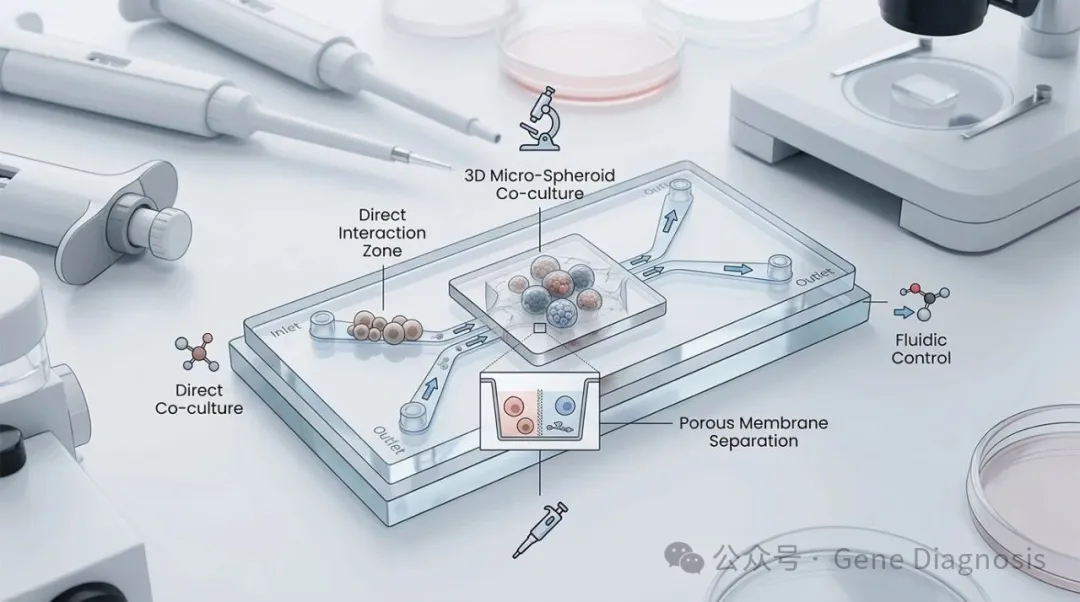
04、微流控芯片共培养 (Microfluidic Co-culture)
原理: 在微米级别的通道内进行培养,通过流体控制精确模拟血液剪切力和营养梯度。
优点: 能够精确控制流体剪切力、氧气浓度梯度;试剂消耗极少(微升级)。
缺点: 装置复杂,通常需要专门的泵系统,通量相对较低。
适用方向: “器官芯片”(Organ-on-a-chip)、血管建模、药物高通量筛选。
★ 选型指南:四大方法横向对比
| 特性 | 直接共培养 | Transwell | 3D共培养 | 微流控芯片 |
| 物理接触 | 是 | 否 | 是/否 | 可控 |
| 细胞回收 | 难(需分选) | 极易 | 较难 | 困难 |
| 体内仿真度 | 一般 | 较低 | 极高 | 高 |
| 操作难度 | ★ | ★★ | ★★★★ | ★★★★★ |
| 核心应用 | 免疫杀伤 | 分泌因子研究 | 组织建模 | 生理流体模拟 |
如果你研究的是“因子分泌”,首选 Transwell。
如果你关注“细胞亲密接触”且不介意后期回收,选 直接共培养。
如果你追求“极致仿真”且经费充足,请挑战 3D 或微流控。
本文由环凯转载自转载自“Gene Diagnosis”公众号,版权归原作者所有,仅供学习参考,如有侵权请联系删除!










