多孔银金微粒+拉曼增强:科学家开发出可同时检测大肠杆菌和金葡菌的新型生物传感器
发布时间:2026-03-18 浏览次数:70 分享:
人类与致病菌的斗争持续存在,复杂的细菌感染威胁着公共健康。早期检测与诊断是预防和治疗复杂病原菌感染最有效的手段之一。然而,传统的检测方法(如平板涂布法、显微镜荧光染色法、聚合酶链式反应和传统免疫测定法)存在各自的局限性,例如耗时长、操作复杂、对实验环境要求高、灵敏度与速度无法兼顾、难以进行现场快速诊断等。
为解决上述问题,即时检验技术应运而生,其中侧流免疫层析(Lateral Flow Immunoassay,LFIA)技术因其快速、简便、成本低而备受关注。但传统LFIA只能进行定性或半定量分析,灵敏度和准确性不足。将表面增强拉曼散射(Surface-Enhanced Raman Scattering,SERS)这一高灵敏度表面技术与LFIA结合,成为研究热点。通过引入新型纳米材料增强SERS信号,可以显著提升检测灵敏度并实现定量分析。因此,合理设计具有高SERS性能的纳米材料探针,并将其成功应用于LFIA平台,以实现对病原菌的现场超灵敏检测,成为本研究的出发点。
本研究由中国科学院海洋研究所的王鹏团队完成。他们通过伽伐尼置换反应合成了一种具有多孔表面的Ag@pore-Au微粒,并将其与Raman染料分子(Cy3/4-MBA)结合,构建了高灵敏度的SERS探针。为了验证该材料的优越性,研究团队对探针进行了系统的表征:透射电子显微镜(TEM)图像(Fig. 1IV)清晰展示了Ag@pore-Au的核壳多孔结构,证明其形成了高密度的“热点”;X射线光电子能谱(XPS, Fig. 1VIII)和X射线衍射图谱(XRD, Fig. 1IX)的测试结果证实了材料中银和金元素的成功复合;动态光散射(DLS)分析(Fig. 1III)确定了探针的粒径分布,而SERS性能测试(Fig. 1V)则证明该结构探针具备极强的信号输出能力,且在PEG包裹后信号稳定性良好。
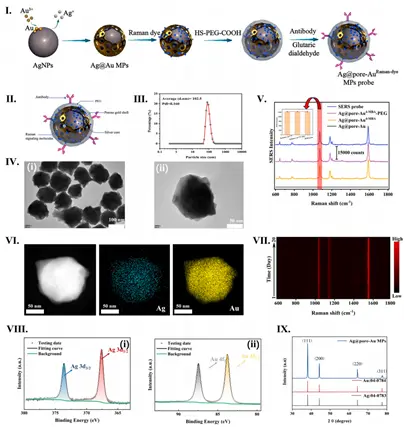
Fig.1 Ag@pore-Au的合成与表征
在应用研究中,团队将上述探针与磁珠分离系统及侧流免疫层析技术相结合,实现了对实际样本中大肠杆菌和金黄色葡萄球菌的双通道检测。研究结果显示,该传感器在最优条件下表现出优异的性能:在磁分离模式下,针对大肠杆菌的特征峰(1586 cm⁻¹)和金葡菌的特征峰(1072 cm⁻¹)均展现出极强的线性关系,线性回归方程分别为y = -1729*x + 10672(R²=0.98)和y = -3855*x + 28751(R²=0.97),检测限均低至10 CFU/mL(Fig. 3III/3V)。在LFIA试纸条应用中,当菌液浓度高于10³ CFU/mL时,T线颜色变化肉眼可见;当浓度低于该阈值时,拉曼检测依然能准确定量(Fig. 4)。在特异性实验中,只有含有对应靶标的实验组才会产生显著SERS信号,且对大肠杆菌和金葡菌的捕获效率分别高达99.4%和98.9%(Fig. 3VII/3IX)。最终,在牛奶、鸡蛋壳和10%人血清的真实样本测试中,回收率均在90.7%至115.0%之间,RSD值也处于合理范围,证明该平台具备良好的抗环境干扰能力和实用性(Fig. 5)。
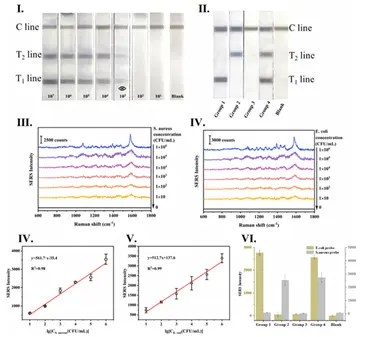
Fig.4 基于Ag@pore-Au Raman-dye MPs探针的侧流免疫层析试纸条的检测灵敏度测试
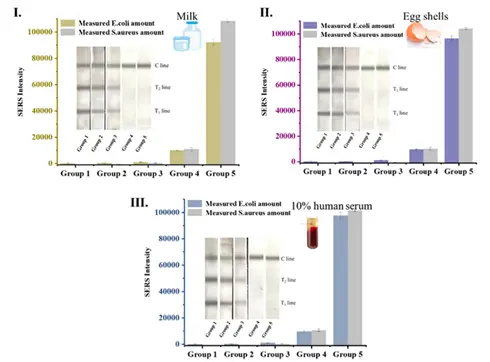
Fig.5 大肠杆菌与金黄色葡萄球菌在牛奶(I)、蛋壳(II)及10%人血清(III)中的实际样品检测
参考文献链接:https://doi.org/10.1016/j.snb.2025.139264
来源:微生物安全与健康网,作者~黃玲。